Berlin (FDP) – Anlässlich der Veröffentlichung des DIMDI-Berichtes zur Antibiotikaabgabe in der Tiermedizin im Jahr 2011 durch das Bundesamt für Verbrauchschutz und Lebensmittelsicherheit, erklärt die agrar- und ernährungspolitische Sprecherin der FDP-Bundestagsfraktion Christel HAPPACH-KASAN:
Antibiotika sind für die Gesunderhaltung unserer Nutz- und Heimtiere wichtige Arzneimittel. Sie schützen vor den Folgen von Infektionserkrankungen. Ihre sachgerechte Anwendung ist ein Gebot des Tierschutzes. Mit der Erhebung des DIMDI (Deutsches Institut für Medizinische Dokumentation und Information) zur Abgabe von Antibiotika an Tierärzte liegen erstmals konkrete Zahlen darüber vor, welche und wie viele Antibiotika in Deutschland an alle Tiere insgesamt abgegeben wurden. In der Erhebung wurde nicht zwischen landwirtschaftlichen Nutztieren und Heimtieren unterschieden. Weitergehende Aussagen zum Antibiotikaeinsatz in der Tierhaltung werden erst möglich sein, wenn alle Zahlen vorliegen.
Positiv hervorzuheben ist, dass humanrelevante Antibiotika, wie Wirkstoffe aus der Gruppe der Fluorchinolone und Cephalosporine, in der Tiermedizin nur in sehr geringem Maße eingesetzt werden.
Die FDP unterstützt die vom Bundesministerium für Ernährung, Landwirtschaft und Verbraucherschutz vorgeschlagenen Änderungen im Arzneimittelgesetz. Es sollen Kennzahlen zum Antibiotikaverbrauch jedes Betriebes erfasst und Betriebe mit überdurchschnittlichem Antibiotikaeinsatz in Zusammenarbeit mit dem betreuenden Tierarzt verpflichtet werden, einen Managementplan zur Reduzierung ihres Medikamenteneinsatzes vorzulegen. Entscheidend für die Gesundheit der Tiere ist gutes, situationsangepasstes Management und nicht die Erreichung von pauschalen Zielvorgaben. Kranke Tiere müssen behandelt werden, Forschung muss möglich bleiben.
In Deutschland werden etwa 40 Millionen Großtiere gehalten (12,6 Mio. Rinder, 26,7 Mio. Schweine, 1 Mio. Pferde) und zusätzlich knapp 800 Millionen Legehennen und Masthähnchen und 27 Millionen Heimtiere wie Hunde und Katzen.

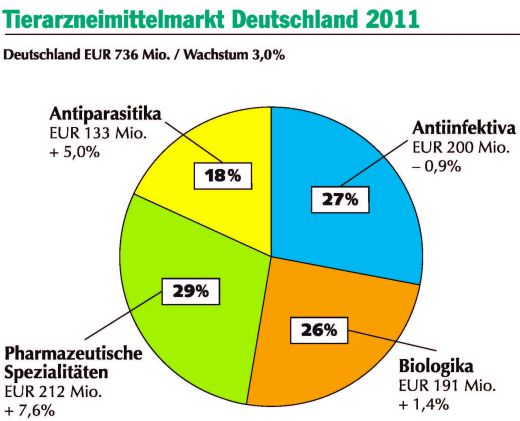 München (aho) – Dr. Martin Schneidereit, Geschäftsführer des Bundesverbandes für Tiergesundheit e.V. (BfT) , erläuterte während der 26. BfT-Mitgliederversammlung am 4. Mai 2012 in München die Marktzahlen für 2011. „Im vergangenen Jahr waren Antiparasitika und Pharmazeutische Spezialitäten die Wachstumstreiber des Tierarzneimittelmarktes. Insgesamt hat sich das Wachstum des Gesamtmarktes auf 736 Mio Euro bei einem Plus von drei Prozent im Vergleich zum Vorjahr weiter abgeschwächt“, so ein Fazit. Die Stagnation des Antibiotikasegmentes habe sich weiter fortgesetzt, erstmalig seien auch Injektionsantibiotika betroffen gewesen. Lediglich Mastitisprodukte und Trockensteller hätten mit mehr als drei Prozent eine erkennbare Aufwärtstendenz gezeigt. „Die verhaltene Marktentwicklung der Antiinfektiva erklärt sich einerseits aus den Unsicherheiten durch die politische Diskussion“, erläuterte Schneidereit diese Entwicklung, „anderseits ist auch eine erhebliche Marktsättigung durch eine Vielzahl von Generikaprodukten zu erkennen“.
München (aho) – Dr. Martin Schneidereit, Geschäftsführer des Bundesverbandes für Tiergesundheit e.V. (BfT) , erläuterte während der 26. BfT-Mitgliederversammlung am 4. Mai 2012 in München die Marktzahlen für 2011. „Im vergangenen Jahr waren Antiparasitika und Pharmazeutische Spezialitäten die Wachstumstreiber des Tierarzneimittelmarktes. Insgesamt hat sich das Wachstum des Gesamtmarktes auf 736 Mio Euro bei einem Plus von drei Prozent im Vergleich zum Vorjahr weiter abgeschwächt“, so ein Fazit. Die Stagnation des Antibiotikasegmentes habe sich weiter fortgesetzt, erstmalig seien auch Injektionsantibiotika betroffen gewesen. Lediglich Mastitisprodukte und Trockensteller hätten mit mehr als drei Prozent eine erkennbare Aufwärtstendenz gezeigt. „Die verhaltene Marktentwicklung der Antiinfektiva erklärt sich einerseits aus den Unsicherheiten durch die politische Diskussion“, erläuterte Schneidereit diese Entwicklung, „anderseits ist auch eine erhebliche Marktsättigung durch eine Vielzahl von Generikaprodukten zu erkennen“.  Leverkusen (Bayer) – Mit BayCubis® 325 mg/g, bisher unter dem Produktnamen Phenoxypen® WSP vertrieben, steht ein effektives, säurestabiles Beta-Lactam-Antibio-tikum von Bayer Tiergesundheit zur Bekämpfung der Nekrotisierenden Enteritis bei Hühnern zur Verfügung. Die durch Clostridium perfringens bedingte Geflügelkrankheit verursacht weltweit immense wirtschaftliche Schäden, da hierdurch sowohl die Mast- als auch die Legeleistung erheblich beeinflusst werden können.
Leverkusen (Bayer) – Mit BayCubis® 325 mg/g, bisher unter dem Produktnamen Phenoxypen® WSP vertrieben, steht ein effektives, säurestabiles Beta-Lactam-Antibio-tikum von Bayer Tiergesundheit zur Bekämpfung der Nekrotisierenden Enteritis bei Hühnern zur Verfügung. Die durch Clostridium perfringens bedingte Geflügelkrankheit verursacht weltweit immense wirtschaftliche Schäden, da hierdurch sowohl die Mast- als auch die Legeleistung erheblich beeinflusst werden können. (BI) – Ab sofort senkt der Impfstoffspezialist Boehringer Ingelheim Vetmedica den Preis für die Ileitisimpfung. Damit ist es möglich die Ileitisimpfung flächendeckend, zusätzlich zu weiteren Impfmaßnahmen zu etablieren – ein Grund mehr, Schweine nachhaltiger und gesünder zu produzieren.
(BI) – Ab sofort senkt der Impfstoffspezialist Boehringer Ingelheim Vetmedica den Preis für die Ileitisimpfung. Damit ist es möglich die Ileitisimpfung flächendeckend, zusätzlich zu weiteren Impfmaßnahmen zu etablieren – ein Grund mehr, Schweine nachhaltiger und gesünder zu produzieren.